เล่ม 3 มวลกับการเกิดปฏิกิริยาเคมี
- 2. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี คานา เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี จัดทาขึ้นเพื่อใช้ประกอบการเรียนรู้สาหรับนักเรียน ชั้นมัธยมศึกษาปีที่ 2 โรงเรียนสีคิ้ว “สวัสดิ์ผดุงวิทยา” ซึ่งเอกสารประกอบการจัดการเรียนรู้นี้ มีจานวน 6 เล่ม เล่มที่ 1 เรื่อง การเกิดปฏิกิริยาเคมี เล่มที่ 2 เรื่อง สมการเคมี เล่มที่ 3 เรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี เล่มที่ 4 เรื่อง ปัจจัยที่มีผลต่อการเกิดปฏิกิริยาเคมี เล่มที่ 5 เรื่อง ปฏิกิริยาเคมีในชีวิตประจาวัน เล่มที่ 6 เรื่อง การใช้สารเคมีอย่างถูกต้องปลอดภัย เอกสารประกอบการจัดกิจกรรมการเรียนรู้นี้จัดทาขึ้นเพื่ออานวยความสะดวกให้ครูและนักเรียน สามารถนาไปใช้ในการจัดกิจกรรมการเรียนรู้ประกอบแผนการจัดการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ในระดับ ชั้นมัธยมศึกษาปีที่ 2 ซึ่งประกอบไป ด้วยแบบทดสอบก่อน - หลังเรียน บันทึกกิจกรรมการทดลอง ใบงานและใบความรู้ ผู้จัดทาหวังเป็นอย่างยิ่งว่า จะเป็นประโยชน์แก่ครูผู้สอน นักเรียนหรือบุคคลที่สนใจทั่วไป ปรีช์ญภัทร เล่งระบา ก
- 3. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี สารบัญ หน้า คานา ก สารบัญ ข แบบทดสอบก่อนเรียน เรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี 1 กิจกรรม 2.2 มวลกับการเกิดปฏิกิริยาเคมี 3 ใบความรู้ที่ 2.3 มวลกับการเกิดปฏิกิริยาเคมี 6 กิจกรรม 2.3 พลังงานกับการเกิดปฏิกิริยาเคมี 9 ใบความรู้ที่ 2.4 พลังงานกับการเกิดปฏิกิริยาเคมี 12 ใบงานที่ 2.3 มวล พลังงานกับการเกิดปฏิกิริยาเคมี 15 แบบทดสอบหลังเรียน เรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี 17 ภาคผนวก 19 ตัวอย่างการบันทึกกิจกรรม 2.2 มวลกับการเกิดปฏิกิริยาเคมี 20 ตัวอย่างการบันทึกกิจกรรม 2.3 พลังงานกับการเกิดปฏิกิริยาเคมี 23 เฉลยใบงานที่ 2.3 มวล พลังงานกับการเกิดปฏิกิริยาเคมี 26 เฉลยข้อสอบก่อนเรียน เรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี 28 เฉลยข้อสอบหลังเรียน เรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี 29 บรรณานุกรม 30 ข
- 4. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี แบบทดสอบก่อนเรียนเรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี คาชี้แจง 1. แบบทดสอบเป็นแบบเลือกตอบ 4 ตัวเลือก จานวน 10 ข้อ ใช้เวลา 10 นาที 2. ให้นักเรียนเลือกคาตอบที่ถูกต้องที่สุดเพียงคาตอบเดียว แล้วทาเครื่องหมาย ลงในกระดาษคาตอบ ************************************************************************************************** 1. ข้อใดกล่าวไม่ถูกต้อง ก. ระบบหมายถึงสิ่งที่เรากาลังศึกษาอยู่ในขณะนั้น ๆ ข. สิ่งแวดล้อมหมายถึงสิ่งต่าง ๆ ที่อยู่นอกขอบเขตของการศึกษา ค. ระบบเปิดหมายถึงระบบที่มีการถ่ายเทมวลสารกับสิ่งแวดล้อม เมื่อเกิดการเปลี่ยนแปลงมวลของ สารในระบบเปลี่ยนแปลงไป ง. ระบบปิดหมายถึงระบบที่มีการถ่ายเทมวลสารกับสิ่งแวดล้อม เมื่อเกิดการเปลี่ยนแปลงมวลของ สารจะคงที่หรือไม่คงที่ก็ได้ 2. ทาการทดลองผสมแคลเซียมไฮดรอกไซด์ Ca(OH)2 กับแอมโมเนียมคลอไรด์ (NH4Cl) เข้าด้วยกันในบีกเกอร์ แล้วใช้แท่งแก้วคนให้เข้ากัน ปรากฏว่าได้แก๊สกลิ่นฉุน วัดอุณหภูมิ ด้วยเทอร์มอมิเตอร์ การทดลองนี้ระบบและสิ่งแวดล้อมคือข้อใด ข้อ ระบบ สิ่งแวดล้อม ก. Ca(OH)2 , NH4Cl, แท่งแก้ว แท่งแก้ว, แก๊สกลิ่นฉุน ข. Ca(OH)2 , NH4Cl, บีกเกอร์ แท่งแก้ว ค. Ca(OH)2 , NH4Cl, แก๊สกลิ่นฉุน บีกเกอร์, เทอร์มอมิเตอร์ ง. Ca(OH)2 , NH4Cl บีกเกอร์, แท่งแก้ว 3. จากวิธีทดลองต่าง ๆ ดังนี้ 1. หยดน้าลงบนโพแทสเซียมไฮดรอกไซด์ 4 กรัม ปรากฏว่าอุณหภูมิของระบบสูงขึ้นกว่าเดิม 2. นาสารที่ได้จากข้อ 1 ไปผสมกับแอมโมเนียมคลอไรด์ 2 กรัม จะได้แก๊สกลิ่นฉุนเกิดขึ้น 3. ผ่านสารที่มีกลิ่นฉุนลงในน้าจะได้สารละลายที่เปลี่ยนสีกระดาษลิตมัสจากแดงเป็นน้าเงิน อุณหภูมิของระบบไม่เปลี่ยนแปลง และยังคงมีกลิ่นฉุนอยู่ การทดลองข้อใดจัดเป็นระบบปิด ก. ข้อ 1 ข. ข้อ 2 ค. ข้อ 1 และ 2 ง. ข้อ 2 และ 3 4. ข้อใดเป็นการเปลี่ยนแปลงในระบบปิด ก. เทกรดซัลฟิวริกลงในน้า เกิดความร้อน ข. การเกิดน้าค้างบนใบไม้ในตอนเช้า ค. เผาลวดแมกนีเซียมในอากาศ ง. การบ่มผลไม้สุก 1
- 5. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี 5. ข้อใดเป็นการเปลี่ยนแปลงในระบบเปิด ก. ผสมสารละลายเลด (II) ไนเตรตกับสารละลายโพแทสเซียมไอโอไดด์เข้าด้วยกัน มีตะกอนสีเหลืองเกิดขึ้น ข. ทิ้งลูกเหม็นไว้ในตู้เสื้อผ้าพบว่ามีขนาดเล็กลง ค. ใส่โซเดียมไนเตรตลงในน้า อุณหภูมิต่าลง ง. เผาแคลเซียมคาร์บอเนตในขวดที่ปิดฝาสนิท 6. ข้อความเกี่ยวกับปฏิกิริยาคายความร้อน ข้อใดถูกต้อง ก. ทาให้สิ่งแวดล้อมมีอุณหภูมิลดลง ข. ต้องใช้ตัวเร่งปฏิกิริยา ค. ตอนเริ่มปฏิกิริยาต้องให้พลังงานเข้าไป ง. สารตั้งต้นมีพลังงานมากกว่าสารผลิตภัณฑ์ 7. ข้อใดถูกต้องเกี่ยวกับปฏิกิริยาดูดความร้อน 1. มีการดูดพลังงานจากสิ่งแวดล้อม 2. มีการปล่อยพลังงานให้กับสิ่งแวดล้อม 3. สิ่งแวดล้อมจะมีอุณหภูมิสูงขึ้น 4. สิ่งแวดล้อมจะมีอุณหภูมิลดลง ก. ข้อ 1 และ 3 ข. ข้อ 1 และ 4 ค. ข้อ 2 และ 3 ง. ข้อ 2 และ 4 8. เมื่อคาร์บอนและออกซิเจนเกิดการรวมตัวกันทางเคมี มวลของผลิตภัณฑ์จะเป็นอย่างไร ก. มากกว่ามวลของคาร์บอนรวมกับมวลของออกซิเจน ข. เท่ากับมวลของคาร์บอนรวมกับมวลของออกซิเจน ค. เท่ากับมวลของคาร์บอน ง. น้อยกว่ามวลของคาร์บอน 9. นักเรียน 2 คน เติมสังกะสีชิ้นหนึ่งในสารละลายกรดไฮโดรคลอริกที่อยู่ในบีกเกอร์ที่เปิดไว้ พบว่ามวลของ ผลิตภัณฑ์น้อยกว่ามวลรวมของสารตั้งต้น ข้อใดอธิบายถึงมวลที่สูญหายไปได้ถูกต้อง ก. โลหะสังกะสีมีความหนาแน่นมากกว่ากรด ข. ความว่องไวต่อปฏิกิริยาเคมีของกรดทาลายอะตอมโลหะ ค. แก๊สชนิดหนึ่งถูกปล่อยออกมาระหว่างปฏิกิริยา ง. อะตอมของสังกะสีบางอะตอมไม่เข้าทาปฏิกิริยา 10. สมการในข้อใดอธิบายถึงกฎทรงมวลของสารได้ดีที่สุด ก. A + 2B AB2 ข. A + 2B AB4 ค. 2A + 2B AB3 ง. A + 3B A2B2 ********************************************************************** 2
- 6. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี กิจกรรม 2.2 มวลกับการเกิดปฏิกิริยาเคมี สมาชิกในกลุ่ม 1. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 2. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 3. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 4. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 5. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 6. ชื่อ..................................................................................................ชั้น.................เลขที่..................... จุดประสงค์ของกิจกรรม เมื่อทากิจกรรมนี้แล้ว นักเรียนควรจะสามารถ 1. ทดลองและอธิบายได้ว่า ผลรวมมวลของสารตั้งต้นที่เข้าทาปฏิกิริยาเคมีเท่ากับผลรวมมวลของสาร ผลิตภัณฑ์ที่เกิดขึ้น 2. อธิบายได้ว่า ในระบบเปิดมวลของสารผลิตภัณฑ์มีการแลกเปลี่ยนกับสิ่งแวดล้อม วัสดุอุปกรณ์และสารเคมี รายการ ปริมาณ/กลุ่ม 1. บีกเกอร์ขนาด 250 cm3 2. หลอดทดลองขนาดกลาง 3. เครื่องชั่ง 4. หลอดทดลองขนาดใหญ่ พร้อมจุกยาง 5. สารละลายแบเรียมคลอไรด์ ความเข้มข้น 0.1 mol/dm3 6. สารละลายโซเดียมซัลเฟต ความเข้มข้น 0.1 mol/dm3 7. สารละลายกรดไฮโดรคลอริก ความเข้มข้น 0.1 mol/dm3 8. เม็ดหินปูนเล็กๆ 1 ใบ 2 หลอด 1 เครื่อง 1 หลอด 5 cm3 5 cm3 10 cm3 2 กรัม (5-8 เม็ด) 3
- 7. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี วิธีทดลอง ตอนที่ 1 1. ชั่งบีกเกอร์ และหลอดทดลอง 2 หลอด โดยหลอดทดลองที่ 1 บรรจุสารละลายแบเรียมคลอไรด์ หลอดทดลองหลอดที่ 2 บรรจุสารละลายโซเดียมซัลเฟต วางในบีกเกอร์และบันทึกมวลของบีกเกอร์ และหลอดทดลองทั้งสองที่บรรจุสารละลายแล้ว 2. เทสารละลายหลอดที่ 1 ลงในหลอดที่ 2 วางหลอดเปล่าไว้ที่เดิม สังเกตการเปลี่ยนแปลง 3. ชั่งบีกเกอร์ และหลอดทดลองทั้งสองอีกครั้ง เปรียบเทียบกับมวลที่ชั่งครั้งแรก การชั่งบีกเกอร์ และหลอดทดลอง 2 หลอด ที่บรรจุสารละลายแล้ว ตอนที่ 2 1. ชั่งบีกเกอร์ ที่ใส่เม็ดหินปูนประมาณ 5 – 8 เม็ด และหลอกทดลองขนาดใหญ่ที่บรรจุสารละลายกรด ไฮโดรคลอริกเจือจาง 10 cm3 พร้อมจุกยางปิดหลอดดังภาพ บันทึกมวล 2. นาเม็ดหินปูนใส่ลงในหลอดทดลองที่บรรจุกรด และปิดจุกยากทันที สังเกตการเปลี่ยนแปลง 3. ตั้งทิ้งไว้จนปฏิกิริยาสิ้นสุด ชั่งบีกเกอร์ และหลอดทดลอง พร้อมจุกยางอีกครั้ง บันทึกมวล 4. เปรียบเทียบมวลที่ชั่งในข้อ 3 กับมวลในข้อ 1 การชั่งบีกเกอร์ที่ใส่เม็ดหินปูน และหลอดทดลองขนาดใหญ่ที่บรรจุกรดแล้ว 4
- 8. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ผลการทดลอง ตอนที่ มวลรวมของสารก่อนนามาผสม (กรัม) มวลรวมของสารหลังผสมกันแล้ว (กรัม) 1 2 คาถามท้ายการทดลอง 1. ในการทดลองตอนที่ 1 มวลของสารก่อนทาปฏิกิริยา และมวลของสารหลังทาปฏิกิริยาเท่ากันหรือไม่ .............................................................................................................................................................. 2. ในการทดลองที่ 2 ถ้าไม่ปิดหลอดทดลองขณะเกิดปฏิกิริยาระหว่างกรดกับหินปูน มวลของสารที่ชั่งได้ ก่อนเกิดปฏิกิริยา และหลังปฏิกิริยาแตกต่างกันหรือไม่ เพราะเหตุใด ............................................................................................................................................................... ............................................................................................................................................................... ............................................................................................................................................................... อภิปรายผลการทดลอง ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… สรุปผลการทดลอง ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… 5
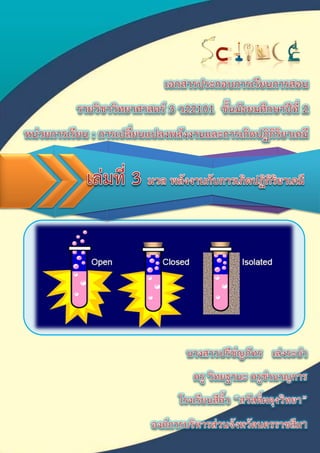
- 9. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ใบความรู้ 2.3 มวลกับการเกิดปฏิกิริยาเคมี ระบบ หมายถึง สิ่งต่าง ๆ ที่อยู่ภายในขอบเขตที่ศึกษา สิ่งแวดล้อม หมายถึง สิ่งต่าง ๆ ที่อยู่นอกขอบเขตที่จะศึกษา ซึ่งอาจจะมีผลต่อระบบหรือไม่ก็ได้ การแบ่งประเภทของระบบ อาศัยมวลและพลังงานเป็นเกณฑ์ สามารถจาแนกได้ดังนี้ 1.ระบบเปิด (Open system) หมายถึง ระบบที่มีการถ่ายเทมวลและพลังงานระหว่างระบบกับ สิ่งแวดล้อม 2.ระบบปิด (Closed system) หมายถึง ระบบที่มีการถ่ายเทพลังงานระหว่างระบบกับสิ่งแวดล้อม แต่ไม่มีการถ่ายเทมวล 3.ระบบอิสระ (Isolated system) หมายถึง ระบบที่ไม่มีการถ่ายเทมวลและพลังงานระหว่าง ระบบกับสิ่งแวดล้อม กล่าวได้ว่าในระบบเปิดทั้งมวลและพลังงานจะไม่คงที่ ในระบบปิดเฉพาะมวลคงที่ และในระบบ อิสระทั้งมวลและพลังงานคงที่ http://thn23217che.blogspot.com/ 6
- 10. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี กฎทรงมวล (Law of mass conservation) กฎทรงมวลเป็นกฎที่ใช้ศึกษาความสัมพันธ์ระหว่างมวลสารก่อนเกิดปฏิกิริยา และมวลสาร ภายหลังเกิดปฏิกิริยา นิยามกฎทรงมวล ในปี ค.ศ. 1774 (พ.ศ. 2317) อองตวน - โลรอง ลาวัวซิเยร์ (Antoine - Lourent Lavoisier) นักเคมีชาวฝรั่งเศส ได้ทาการทดลองเผาเมอร์คิวรี (II) ออกไซด์ (HgO) ซึ่งเป็นของแข็งในภาชนะปิด พบว่าได้ ปรอทและแก๊สออกซิเจน จากการศึกษา “มวลของ HgO เท่ากับผลบวกของ Hg กับ O2” จึงได้สรุปเป็น กฎทรงมวล ว่า “ในปฏิกิริยาเคมีใดๆ มวลของสารทั้งหมดก่อนทาปฏิกิริยาเท่ากับมวลของสารทั้งหมดหลังทาปฏิกิริยา” มวลของสารก่อนทาปฏิกิริยา หมายถึง มวลของสารทั้งหมดตอนเริ่มต้นของปฏิกิริยา มวลของ สารเหล่านี้อาจจะทาปฏิกิริยาพอดีกัน หรืออาจจะมีสารใดเหลืออยู่ก็ได้ มวลของสารหลังทาปฏิกิริยา หมายถึง มวลของสารทั้งหมดหลังจากเกิดปฏิกิริยาแล้ว ทั้งมวล ของผลิตภัณฑ์ทั้งหมด และมวลของสารตั้งต้นที่ยังเหลืออยู่ ดังนั้น ในทางปฏิบัติ ข้อมูลจะเป็นไปตามกฎทรงมวลได้ต้องทาการทดลองในระบบปิดเท่านั้น ในกรณีที่มีแก๊สเกี่ยวข้องในระบบด้วยนั้นจะต้องทาการทดลองในภาชนะปิดฝา จึงจะได้ผลตามกฎทรงมวล ตัวอย่าง 1 ปฏิกิริยาระหว่างสารละลายโพแทสเซียมไอโอไดด์(KI) มวล 10 กรัม กับสารละลายเลด(II) ไนเตรต (Pb(NO3)2) มวล 20 กรัม ได้ตะกอนสีเหลืองของเลด(II)ไอโอไดด์ (PbI2) กับสารละลายโพแทสเซียม ไนเตรต(KNO3) ซึ่งมีมวลรวมกัน 30 กรัม ซึ่งจะเห็นว่ามวลรวมของสารก่อนทาปฏิกิริยา( 10 + 20 = 30 กรัม) เท่ากับมวลรวมของสารหลังทาปฏิกิริยา(30 กรัม) ปฏิกิริยานี้จึงจัดเป็น “ระบบปิด” https://socratic.org/questions/considering-the-following-precipitation-reaction-pb-no3-2-aq-2ki-aq-pbi2-s-2kno3 7
- 11. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ตัวอย่าง 2 ปฏิกิริยาระหว่างผงฟู(NaHCO3) กับน้าส้มสายชู(CH3COOH) มีมวลรวมก่อนทาปฏิกิริยา 3.861 กรัม หลังทาปฏิกิริยาเกิดเกลือโซเดียมอะซิเตต น้าและแก๊สคาร์บอนไดออกไซด์ มีมวลรวมกัน 3.861 กรัม ซึ่งจะเห็นว่ามวลรวมของสารก่อนทาปฏิกิริยาเท่ากับมวลรวมของสารหลังทาปฏิกิริยาปฏิกิริยานี้ จึงจัดเป็น “ระบบปิด” ตัวอย่าง 3 การเกิดปฏิกิริยาระหว่างกรดไฮโดรคลอริก มวล 10 กรัม กับโพแทสเซียมไฮโดรเจน คาร์บอเนต มวล 1 กรัมโดยไม่ได้ปิดจุกคอร์ก หลังเกิดปฏิกิริยาได้ เกลือโพแทสเซียมคลอไรด์ แก๊สคาร์บอนไดออกไซด์และน้า มีมวลรวมหลังเกิดปฏิกิริยา 10.5 กรัม ซึ่งจะเห็นว่ามวลรวมของสาร ก่อนทาปฏิกิริยาไม่เท่ากับมวลรวมของสารหลังทาปฏิกิริยา แสดงว่ามีการถ่ายเทมวลสาร(แก๊ส)ให้กับ สิ่งแวดล้อม ปฏิกิริยานี้จึงจัดเป็น “ระบบเปิด” http://www.harpercollege.edu/tm-ps/chm/100/dgodambe/thedisk/chemrxn/jrxn.jpg ทั้งระบบเปิด และระบบปิด อาจมีการถ่ายเทพลังงาน กับสิ่งแวดล้อมหรือไม่ก็ได้ การพิจารณาว่า ระบบใดเป็นระบบเปิด-ปิดนั้น บางครั้งการพิจารณาภาชนะของระบบนั้นก็จะทาให้เข้าใจง่ายขึ้น ซึ่งมีหลัก ดังนี้ ระบบใด ๆ ที่เกิดขึ้นโดยทั่วไปนั้นกระทาในภาชนะ 2 ประเภท คือ ภาชนะเปิดกับภาชนะปิด (เปิดฝากับปิดฝาภาชนะ) ระบบใดก็ตามที่ไม่มีแก๊ส เกี่ยวข้องเลย การปิด-เปิดภาชนะไม่มีผลต่อชนิดของระบบแต่อย่างใด ถ้าระบบใดๆ ที่มีแก๊สเกี่ยวข้องอยู่ด้วย การปิด-เปิดภาชนะจะมีผลต่อชนิดของระบบนั้นด้วย กล่าวคือ 3.1 ถ้าเปิดภาชนะ (เปิดฝา) ระบบนั้นก็เป็นระบบเปิด เพราะมวลเปลี่ยนแปลง (แก๊สหนีออกไป) 3.2 ถ้าปิดภาชนะ (ปิดฝา) ระบบนั้นก็เป็นระบบปิด เพราะมวลคงที่ (แก๊สหนีออกไม่ได้) https://sites.google.com/site/benarabifq/1o-de-bachillerato/quimica/2---fundamentos-de-la-quimica 8
- 12. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี กิจกรรม 2.3 พลังงานกับการเกิดปฏิกิริยาเคมี สมาชิกในกลุ่ม 1. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 2. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 3. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 4. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 5. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 6. ชื่อ..................................................................................................ชั้น.................เลขที่..................... จุดประสงค์ของกิจกรรม เมื่อทากิจกรรมนี้แล้ว นักเรียนควรจะสามารถ 1. ทดลองและอธิบายได้ว่า ในการเกิดปฏิกิริยาเคมีจะมีพลังงานเข้ามาเกี่ยวข้อง 2. อธิบายเกี่ยวกับปฏิกิริยาดูดพลังงานและปฏิกิริยาคายพลังงานได้ วัสดุอุปกรณ์และสารเคมี รายการ ปริมาณ/กลุ่ม 1. ถ้วยกระเบื้อง 2. แท่งแก้วคนสาร 3. หลอดหยด 4. โพแทสเซียมเปอร์แมงกาเนต 5. น้าตาลทราย 6. แคลเซียมไฮดรอกไซด์ 7. แอมโมเนียมคลอไรด์ 8. น้ากลั่น 9. กระดาษลิตมัสสีแดงและสีน้าเงิน 10. ช้อนเบอร์ 1 2 ถ้วย 2 อัน 1 อัน 2 ช้อนเบอร์ 1 2 ช้อนเบอร์ 1 2 ช้อนเบอร์ 1 2 ช้อนเบอร์ 1 50 cm3 2 ชิ้น 4 อัน 9
- 13. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี วิธีทดลอง ตอนที่ 1 1. ผสมโพแทสเซียมเปอร์แมงกาเนตและน้าตาลทรายอย่างละ 2 ช้อน ในถ้วยกระเบื้อง 2. หยดน้าลงไป 3 – 5 หยด ใช้แท่งแก้วคนสาร สังเกตการเปลี่ยนแปลงและเอามือสัมผัสบริเวณด้าน นอกถ้วยกระเบื้องด้วยความระมัดระวัง ตอนที่ 2 1. ผสมสารแคลเซียมไฮดรอกไซด์กับแอมโมเนียมคลอไรด์อย่างละ 2 ช้อนในถ้วยกระเบื้อง 2. หยดน้าลงไป 3 – 5 หยด ใช้แท่งแก้วคนสาร สังเกตการเปลี่ยนแปลงและเอามือสัมผัสบริเวณด้าน นอกถ้วยกระเบื้องด้วยความระมัดระวัง 3. ใช้กระดาษลิตมัสชื้นอังเหนือบีกเกอร์ สังเกตและบันทึกผล ผลการทดลอง ตอนที่ การเกิดปฏิกิริยาของสาร ผลการสังเกต 1 โพแทสเซียมเปอร์แมงกาเนต + น้าตาลทราย 2 แคลเซียมไฮดรอกไซด์ + แอมโมเนียมคลอไรด์ คาถามท้ายการทดลอง 1. ในการทดลองนี้มีปฏิกิริยาเกิดขึ้นหรือไม่ ทราบได้อย่างไร .............................................................................................................................................................. .............................................................................................................................................................. .............................................................................................................................................................. .............................................................................................................................................................. 2. ในการทดลองที่ 1 เป็นการเปลี่ยนแปลงพลังงานประเภทใด เพราะเหตุใด ............................................................................................................................................................... ............................................................................................................................................................... ............................................................................................................................................................... 10
- 14. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี 3. ในการทดลองที่ 2 เป็นการเปลี่ยนแปลงพลังงานประเภทใด เพราะเหตุใด ............................................................................................................................................................... ............................................................................................................................................................... ............................................................................................................................................................... 4. แก๊สที่ได้จากการทดลองตอนที่ 2 มีสมบัติเป็นกรดหรือเป็นเบส สังเกตได้จากอะไร ............................................................................................................................................................... ............................................................................................................................................................... ............................................................................................................................................................... อภิปรายผลการทดลอง ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… สรุปผลการทดลอง ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………………………………………………… 11
- 15. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ใบความรู้ที่ 2.4 พลังงานกับการเกิดปฏิกิริยาเคมี การเกิดปฏิกิริยาเคมีนั้นจะมีการเปลี่ยนแปลงพลังงานเสมอ รวมทั้งมีการเปลี่ยนแปลงอุณหภูมิด้วย ซึ่งอุณหภูมิอาจเพิ่มขึ้นหรือลดลง เนื่องมาจากเกิดจากการถ่ายเทพลังงานจากระดับพลังงานที่สูงกว่า ไปสู่ ระดับพลังงานที่ต่ากว่า ดังนั้นการเกิดปฏิกิริยาเคมีต่างๆ จะประกอบไปด้วย กระบวนการที่สาคัญ 2 กระบวนการ ได้แก่ กระบวนการดูดพลังงานเพื่อสลายพันธะของสารตั้งต้น และกระบวนการคายพลังงาน เพื่อสร้างพันธะของสารผลิตภัณฑ์ ถ้าพลังงานที่ดูดเข้าไปเพื่อสลายพันธะของสารตั้งต้นน้อยกว่า พลังงานที่คาย ออกมาเพื่อสร้างพันธะใหม่ ก็จะเป็นปฏิกิริยาคายความร้อน แต่ถ้าพลังงานที่ดูดเข้าไปเพื่อสลายพันธะของสาร ตั้งต้นมากกว่าพลังงานที่ คายออกมาเพื่อสร้างพันธะใหม่ ก็จะเป็นปฏิกิริยาดูดความร้อน 1) ปฏิกิริยาดูดความร้อน (endothermic reaction) คือ ปฏิกิริยาที่ ระบบมีอุณหภูมิลดต่าลง จึงดูด พลังงานความร้อนจากสิ่งแวดล้อม ทาให้สิ่งแวดล้อมมีอุณหภูมิต่าลง เมื่อใช้มือสัมผัสกับภาชนะที่เกิดปฏิกิริยา จะรู้สึกเย็น แต่หลังจากปฏิกิริยาสิ้นสุดลงระบบจะมีอุณหภูมิสูงขึ้น https://kruwichailikitponrak.wordpress.com/11-การสังเคราะห์ด้วยแสง/ 2) ปฏิกิริยาคายความร้อน (exothermic reaction) คือ ปฏิกิริยา ที่ขณะเกิดปฏิกิริยาจะมีพลังงาน เกิดขึ้น ระบบจึงมีอุณหภูมิสูง จึงคายพลังงานความร้อนออกสู่สิ่งแวดล้อม ซึ่งเมื่อใช้มือสัมผัสกับภาชนะที่ เกิดปฏิกิริยาจะรู้สึกร้อน แต่หลังจากปฏิกิริยาสิ้นสุดลงระบบจะมีอุณหภูมิลดต่าลง https://commons.wikimedia.org/wiki/File:KMnO4_and_glycerol.jpg 12
- 16. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ความรู้เพิ่มเติม การเกิดปฏิกิริยาเคมีในบางครั้งไมไดตองการผลิตภัณฑ์ที่เกิดขึ้น แต่ต้องการที่ปริมาณความร้อนที่ ปฏิกิริยานั้นให้ออกมาเป็นจานวนมาก เช่น ปฏิกิริยาการเผาไหมของเชื้อเพลิงฟอสซิล แก๊สธรรมชาติ แก๊สหุงต้ม น้ามันเบนซิน น้ามันดีเซล เป็นต้น ก่อนปฏิกิริยาจะเกิดขึ้นต้องให้ความร้อนแกเชื้อเพลิงจานวนหนึ่ง เมื่อเชื้อเพลิงเกิดการเผาไหมแล้วจึงให้ความร้อนออกมาในปริมาณมาก การวิเคราะห์ปริมาณความร้อนที่ เกิดขึ้นจากปฏิกิริยาต้องคานึงถึง “ระบบ” และ “สิ่งแวดล้อม” ระบบในทางเคมีนั้นจะหมายถึงสารตั้งต้น สาร ผลิตภัณฑ์และสารอื่นๆ ที่เกี่ยวข้องกับการเกิดปฏิกิริยา นอกเหนือจากนั้นเรียกว่า สิ่งแวดล้อม เช่น การเผา ไหม้ แกสมีเทน ในอากาศ ดังสมการ CH4 + 2O2 CO2 + 2H2O แกสมีเทน แกสออกซิเจน แก๊สคารบอนไดออกไซด น้า ระบบในที่นี้หมายถึงแกสมีเทน แกสออกซิเจน แก๊สคาร์บอนไดออกไซด์ และน้า สวนอื่นๆ นอกเหนือจากนี้ เป็นสิ่งแวดล้อม โดยทั่วไป ระบบมีอยู่ 3 แบบคือ ระบบปิด ระบบเปิด ระบบโดดเดี่ยว ระบบเปิดเป็นระบบที่มีการแลกเปลี่ยนมวลสารและความร้อน เช่น ปฏิกิริยาระหว่างสังกะสีกับกรด ไฮโดร คลอริกในหลอดทดลองที่ไมมีจุกยางปิด มวลของไฮโดรเจนที่เกิดขึ้นจะแพรกระจายสูอากาศที่เป็น สิ่งแวดล้อม มีการแลกเปลี่ยนความร้อนกับหลอดทดลองและอากาศโดยรอบ ระบบปิดเป็นระบบที่ไมมีการแลกเปลี่ยนมวลสารกับสิ่งแวดล้อมแต่สามารถแลกเปลี่ยนความร้อนกับ สิ่งแวดล้อมได เช่น ปฏิกิริยาระหว่างสังกะสีกับกรดไฮโดรคลอริกในหลอดทดลองที่มีจุกยางปิด มวลของ ไฮโดรเจน ที่เกิดขึ้นไมหายไปไหนยังอยู่ในหลอดทดลอง และมีการแลกเปลี่ยนความร้อนกับหลอดทดลองและ อากาศโดยรอบ ระบบโดดเดี่ยวเป็น ระบบที่ไม่มีการแลกเปลี่ยนมวลสารและความร้อนกับสิ่งแวดล้อม เช่น ปฏิกิริยา ระหว่าง สังกะสีกับกรดไฮโดรคลอริกในหลอดทดลองที่มีจุกยางปิดแล้วห่อหุ้มด้วยฉนวนไมให้ความร้อนที่ เกิดขึ้นไปไหน มวลของไฮโดรเจนที่เกิดขึ้นและความร้อนไมแลกเปลี่ยนกับอากาศ (ถาอนุโลมให้หลอดแก้วและ จุกยางเป็นส่วนหนึ่งของระบบ แต่ในความเป็นจริงหลอดแก้วและจุกยางก็เป็นสิ่งแวดล้อม จึงมีการแลกเปลี่ยน ความร้อนกับ สารที่อยู่ในหลอดแกว ดังนั้น ระบบโดดเดี่ยวจึงเป็นไปไดยาก) จากการพิจารณาความสัมพันธ์ระหว่างระบบสิ่งแวดล้อมและปริมาณความร้อนของปฏิกิริยาเคมีนั้น เป็นไปได 2 กรณี คือ ระบบไดรับปริมาณความร้อนจากสิ่งแวดล้อมมากกว่าปริมาณความร้อนที่ระบบให้คืนกับ สิ่งแวดล้อมเมื่อสิ้นสุดปฏิกิริยา ซึ่งจะเกิดจากปฏิกิริยาดูดความร้อน ในทางตรงกันข้าม ถ้าเป็นปฏิกิริยาคาย ความร้อน ปริมาณความร้อนที่ระบบคืนให้กับสิ่งแวดล้อมเมื่อสิ้นสุดปฏิกิริยามากกว่าปริมาณความร้อน ที่ ระบบไดรับจากสิ่งแวดล้อม ตัวอย่างปฏิกิริยาแบบดูดความร้อน อุณหภูมิของสิ่งแวดล้อมจะมีอุณหภูมิต่าลง บางปฏิกิริยาต้องมี การ ให้ความร้อนแกสารตลอดเวลาสารจึงจะเกิดการสลายตัว ตัวอย่างปฏิกิริยาแบบนี้ เช่น ปฏิกิริยาระหว่าง กรดซิตริก กับโซเดียมไฮโดรเจนคาร์บอเนต ปฏิกิริยาเผาสลายหินปูนเพื่อให้ไดปูนขาว ปฏิกิริยาแบบคายความร้อน อุณหภูมิของสิ่งแวดล้อมจะสูงขึ้น ตัวอย่างปฏิกิริยาแบบนี้ เช่น ปฏิกิริยา การเผาไหม จะมีความร้อนที่ระบบให้ออกมาจานวนมากโดยที่เราจุดไฟให้ในตอนเริ่มต้นเพียงเล็กน้อยเท่านั้น ปฏิกิริยาก็เกิดขึ้นไดตลอดจนกว่าเชื้อเพลิงหมดไป ต่างกับการเผาหินปูน หากไมมีความร้อนที่ใช้เผาแล้วหินปูน ก็จะไมเกิดการสลายตัวให้ปูนขาว 13
- 17. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี การเกิดปฏิกิริยาเคมีของสารนั้น สามารถอธิบายไดด้วยทฤษฎีการชน (collision theory) ซึ่งอธิบาย ถึง การเกิดปฏิกิริยาของสารว่า ปฏิกิริยาเคมีเกิดขึ้นไดเนื่องจากการชนกันของโมเลกุลของสารตั้งต้น เช่น โมเลกุล A ชนกับโมเลกุล B ซึ่งในความเป็นจริงการชนกันแต่ละครั้งไมไดเกิดปฏิกิริยาทุกครั้ง จากการคานวณ ตามทฤษฎี พบว่า ที่ความดัน 1 บรรยากาศ 25๐ C โมเลกุลของแก๊สที่ 22.4 dm3 จะชนกันประมาณ 1 x 1027 ครั้ง/วินาที การชนกันของโมเลกุลที่จะเกิดปฏิกิริยาไดนั้น โมเลกุลของสารจะต้องมีพลังงานจลน์ที่สูง พอและมีทิศทางการชน ที่เหมาะสม สารแต่ละโมเลกุลไมไดมีพลังงานจลน์เท่ากันทุกโมเลกุล มีบางส่วนที่มี พลังงานจลน์มาก บางส่วนมีพลังงานจลน์น้อย การที่โมเลกุลชนกันแล้วเกิดปฏิกิริยาไดนั้นต้องมีพลังงานจลน์ รวมกันแลวอย่างน้อยเท่ากับพลังงานก่อกัมมันต์ (activation energy : Ea) ซึ่งเป็นพลังงานต่าสุดที่ทาให้ เกิดปฏิกิริยาได ถ้ามีพลังงานต่ากว่าพลังงานก่อกัมมันต์ โมเลกุลจะไมมีการเปลี่ยนแปลงหลังการชนกัน โมเลกุลของสารตั้งต้นที่ชนกันแล้วเกิดปฏิกิริยาเคมีนั้น จะรวมตัวเป็นสารเชิงซ้อนกัมมันต์ (activated complex) ซึ่งจะอยู่ได้เพียงชั่วขณะ แลวจะกลายเป็นสารผลิตภัณฑ์ สารจะเกิดปฏิกิริยาต้องได้รับพลังงาน เข้าไปจานวนหนึ่งในปริมาณต่าสุดเท่ากับพลังงานก่อกัมมันต์ เมื่อสารเกิดปฏิกิริยาแล้วจะให้พลังงานออกมา จานวนหนึ่ง ซึ่งอาจมากกว่าหรือน้อยกว่าพลังงานก่อกัมมันต์ก็ได้ พลังงานที่ได้รับและให้ออกมาอาจเป็น ปริมาณความร้อน ถ้าความร้อนที่ไดรับเข้าไปมีมากกว่าความร้อนที่ให้ออกมาก็เป็น ปฏิกิริยาดูดความร้อน ถ้าความร้อนที่ไดรับเข้าไปมีน้อยกว่าความร้อนที่ให้ออกมาก็เป็นปฏิกิริยาคายความร้อน ข้อมูลจาก : หนังสือคู่มือครู รายวิชาวิทยาศาสตร์พื้นฐาน วิทยาศาสตร์ 3 ม.2 เล่ม 1 ตามหลักสูตรแกนกลางการศึกษาขั้นพื้นฐาน พุทธศักราช 2551 (หน้า 43-44) 14
- 18. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ใบงานที่ 2.3 มวล พลังงานกับการเกิดปฏิกิริยาเคมี ใช้ข้อมูลต่อไปนี้ตอบคาถามข้อ 1-3 ในการศึกษาการละลายของโซเดียมไฮดรอกไซด์ในน้าโดยเติมน้าลงในบีกเกอร์จานวน 100 cm3 วัดอุณหภูมิของน้าด้วยเทอร์มอมิเตอร์ได้ 25 องศาเซลเซียส จากนั้นนาโซเดียมไฮดรอกไซด์ จานวน 5 กรัม ใส่ลงในบีกเกอร์และใช้แท่งแก้วคนจนโซเดียมไฮดรอกไซด์ละลายหมดจึงวัดอุณหภูมิได้ 40 องศาเซลเซียส 1. จากการศึกษาดังกล่าวสิ่งใดคือระบบ ตอบ .........................................………………………………………………………………………………………………… 2. การศึกษาการละลายของโซเดียมไฮดรอกไซด์ในน้าครั้งนี้สิ่งใดคือสิ่งแวดล้อม ตอบ .........................................………………………………………………………………………………………………… 3. การละลายของโซเดียมไฮดรอกไซด์นี้เป็นการเปลี่ยนแปลงแบบใด ตอบ .........................................………………………………………………………………………………………………… ใช้ข้อมูลต่อไปนี้ตอบคาถามข้อ 4-6 4. จากการทดลองดังกล่าวสิ่งใดคือระบบ ตอบ .........................................………………………………………………………………………………………………… 5. จากการทดลองผสมแคลเซียมไฮดรอกไซด์ Ca(OH)2 กับแอมโมเนียมคลอไรด์ (NH4Cl) ครั้งนี้สิ่งใดคือ สิ่งแวดล้อม ตอบ .........................................………………………………………………………………………………………………… 6. การทดลองนี้เป็นการเปลี่ยนแปลงแบบใด ตอบ .........................................………………………………………………………………………………………………… 7. ปฏิกิริยาเคมีที่มีการถ่ายเทพลังงานให้กับสิ่งแวดล้อมเป็นปฏิกิริยาเคมีแบบใด ตอบ .........................................………………………………………………………………………………………………… 8. ปฏิกิริยาเคมีที่มีการดูดพลังงานจากสิ่งแวดล้อมเป็นปฏิกิริยาเคมีแบบใด ตอบ .........................................………………………………………………………………………………………………… 9. ให้สาร A ทาปฏิกิริยากับสาร B 10 กรัม ในบีกเกอร์ที่มีฝาปิด เกิดเป็นสาร C จานวน 8 กรัม และแก๊ส D 6 กรัม ถ้าการทดลองนี้เป็นไปตามกฎทรงมวลแสดงว่าปฏิกิริยานี้ใช้สาร A กี่กรัม ตอบ .........................................………………………………………………………………………………………………… 10. เผาคาร์บอน 24 กรัม ในภาชนะที่ปิดฝาสนิท เมื่อสิ้นสุดปฏิกิริยาพบว่าเกิดแก๊สคาร์บอนไดออกไซด์ขึ้น 88 กรัม อยากทราบว่าปฏิกิริยานี้ใช้แก๊สออกซิเจนกี่กรัม ตอบ .........................................………………………………………………………………………………………………… จากการทดลองผสมแคลเซียมไฮดรอกไซด์ Ca(OH)2 กับแอมโมเนียมคลอไรด์ (NH4Cl) เข้าด้วยกัน ในบีกเกอร์ แล้วใช้แท่งแก้วคนให้เข้ากัน ปรากฏว่าได้แก๊สกลิ่นฉุน วัดอุณหภูมิด้วยเทอร์มอมิเตอร์พบว่ามี อุณหภูมิลดลง 2 องศาเซลเซียส 15
- 19. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี 11. ผู้ที่ทาการทดลองและให้ข้อสรุปเกี่ยวกับกฎทรงมวล คือนักเคมีชาวฝรั่งเศส มีชื่อว่า ................................................................................................................................................................ 12. กฎทรงมวล สรุปไว้ว่าอย่างไร ............................................................................................................................................................... ............................................................................................................................................................... 13. ผลการทดลองใด ๆ จะเป็นไปตามกฎทรงมวลจะต้องทาการทดลองในระบบใด ............................................................................................................................................................... 14. ถ้าในการทดลองมีแก๊สเกิดขึ้น จะต้องมีการจัดเตรียมการทดลองอย่างไรให้เป็นไปตามกฎทรงมวล ............................................................................................................................................................... ............................................................................................................................................................... 15. จากการทดลองในข้อที่ 10 ถ้าเราไม่ได้ปิดฝาภาชนะ มวลของสารหลังทาปฏิกิริยาจะมีปริมาณ เปลี่ยนแปลงไปอย่างไร เพราะเหตุใด ............................................................................................................................................................... ............................................................................................................................................................... ............................................................................................................................................................... *********************************************************** 16
- 20. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี แบบทดสอบหลังเรียนเรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี คาชี้แจง 1. แบบทดสอบเป็นแบบเลือกตอบ 4 ตัวเลือก จานวน 10 ข้อ ใช้เวลา 10 นาที 2. ให้นักเรียนเลือกคาตอบที่ถูกต้องที่สุดเพียงคาตอบเดียว แล้วทาเครื่องหมาย ลงในกระดาษคาตอบ ************************************************************************************************** 1. ข้อใดเป็นการเปลี่ยนแปลงในระบบเปิด ก. ผสมสารละลายเลด(II)ไนเตรตกับสารละลายโพแทสเซียมไอโอไดด์เข้าด้วยกัน มีตะกอนสีเหลืองเกิดขึ้น ข. ทิ้งลูกเหม็นไว้ในตู้เสื้อผ้าพบว่ามีขนาดเล็กลง ค. ใส่โซเดียมไนเตรตลงในน้า อุณหภูมิต่าลง ง. เผาแคลเซียมคาร์บอเนตในขวดที่ปิดฝาสนิท 2. สมการในข้อใดอธิบายถึงกฎทรงมวลของสารได้ดีที่สุด ก. A + 2B AB2 ข. A + 2B AB4 ค. 2A + 2B AB3 ง. A + 3B A2B2 3. ข้อความเกี่ยวกับปฏิกิริยาคายความร้อน ข้อใดถูกต้อง ก. ทาให้สิ่งแวดล้อมมีอุณหภูมิลดลง ข. ต้องใช้ตัวเร่งปฏิกิริยา ค. ตอนเริ่มปฏิกิริยาต้องให้พลังงานเข้าไป ง. สารตั้งต้นมีพลังงานมากกว่าสารผลิตภัณฑ์ 4. ข้อใดกล่าวไม่ถูกต้อง ก. ระบบหมายถึงสิ่งที่เรากาลังศึกษาอยู่ในขณะนั้น ๆ ข. สิ่งแวดล้อมหมายถึงสิ่งต่าง ๆ ที่อยู่นอกขอบเขตของการศึกษา ค. ระบบเปิดหมายถึงระบบที่มีการถ่ายเทมวลสารกับสิ่งแวดล้อม เมื่อเกิดการเปลี่ยนแปลงมวลของ สารในระบบเปลี่ยนแปลงไป ง. ระบบปิดหมายถึงระบบที่มีการถ่ายเทมวลสารกับสิ่งแวดล้อม เมื่อเกิดการเปลี่ยนแปลงมวลของ สารจะคงที่หรือไม่คงที่ก็ได้ 5. นักเรียน 2 คน เติมสังกะสีชิ้นหนึ่งในสารละลายกรดไฮโดรคลอริกที่อยู่ในบีกเกอร์ที่เปิดไว้ พบว่ามวลของ ผลิตภัณฑ์น้อยกว่ามวลรวมของสารตั้งต้น ข้อใดอธิบายถึงมวลที่สูญหายไปได้ถูกต้อง ก. โลหะสังกะสีมีความหนาแน่นมากกว่ากรด ข. ความว่องไวต่อปฏิกิริยาเคมีของกรดทาลายอะตอมโลหะ ค. แก๊สชนิดหนึ่งถูกปล่อยออกมาระหว่างปฏิกิริยา ง. อะตอมของสังกะสีบางอะตอมไม่เข้าทาปฏิกิริยา 17
- 21. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี 6. ข้อใดถูกต้องเกี่ยวกับปฏิกิริยาดูดความร้อน 1. มีการดูดพลังงานจากสิ่งแวดล้อม 2. มีการปล่อยพลังงานให้กับสิ่งแวดล้อม 3. สิ่งแวดล้อมจะมีอุณหภูมิสูงขึ้น 4. สิ่งแวดล้อมจะมีอุณหภูมิลดลง ก. ข้อ 1 และ 3 ข. ข้อ 1 และ 4 ค. ข้อ 2 และ 3 ง. ข้อ 2 และ 4 7. ข้อใดเป็นการเปลี่ยนแปลงในระบบปิด ก. เทกรดซัลฟิวริกลงในน้า เกิดความร้อน ข. การเกิดน้าค้างบนใบไม้ในตอนเช้า ค. เผาลวดแมกนีเซียมในอากาศ ง. การบ่มผลไม้สุก 8. จากวิธีทดลองต่าง ๆ ดังนี้ 1. หยดน้าลงบนโพแทสเซียมไฮดรอกไซด์ 4 กรัม ปรากฏว่าอุณหภูมิของระบบสูงขึ้นกว่าเดิม 2. นาสารที่ได้จากข้อ 1 ไปผสมกับแอมโมเนียมคลอไรด์ 2 กรัม จะได้แก๊สกลิ่นฉุนเกิดขึ้น 3. ผ่านสารที่มีกลิ่นฉุนลงในน้าจะได้สารละลายที่เปลี่ยนสีกระดาษลิตมัสจากแดงเป็นน้าเงิน อุณหภูมิของระบบไม่เปลี่ยนแปลง และยังคงมีกลิ่นฉุนอยู่ การทดลองข้อใดจัดเป็นระบบปิด ก. ข้อ 1 ข. ข้อ 2 ค. ข้อ 1 และ 2 ง. ข้อ 2 และ 3 9. เมื่อคาร์บอนและออกซิเจนเกิดการรวมตัวกันทางเคมี มวลของผลิตภัณฑ์จะเป็นอย่างไร ก. มากกว่ามวลของคาร์บอนรวมกับมวลของออกซิเจน ข. เท่ากับมวลของคาร์บอนรวมกับมวลของออกซิเจน ค. เท่ากับมวลของคาร์บอน ง. น้อยกว่ามวลของคาร์บอน 10. ทาการทดลองผสมแคลเซียมไฮดรอกไซด์ Ca(OH)2 กับแอมโมเนียมคลอไรด์ (NH4Cl) เข้าด้วยกันในบีกเกอร์ แล้วใช้แท่งแก้วคนให้เข้ากัน ปรากฏว่าได้แก๊สกลิ่นฉุน วัดอุณหภูมิ ด้วยเทอร์มอมิเตอร์ การทดลองนี้ระบบและสิ่งแวดล้อมคือข้อใด ข้อ ระบบ สิ่งแวดล้อม ก. Ca(OH)2 , NH4Cl, แท่งแก้ว แท่งแก้ว, แก๊สกลิ่นฉุน ข. Ca(OH)2 , NH4Cl, บีกเกอร์ แท่งแก้ว ค. Ca(OH)2 , NH4Cl, แก๊สกลิ่นฉุน บีกเกอร์, เทอร์มอมิเตอร์ ง. Ca(OH)2 , NH4Cl บีกเกอร์, แท่งแก้ว ********************************************************************** 18
- 22. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี 19 ตัวอย่างการบันทึกกิจกรรม 2.2 มวลกับการเกิดปฏิกิริยาเคมี ตัวอย่างการบันทึกกิจกรรม 2.3 พลังงานกับการเกิดปฏิกิริยาเคมี ใบงานที่ 2.3 มวล พลังงานกับการเกิดปฏิกิริยาเคมี เฉลยข้อสอบก่อนเรียน มวล พลังงานกับการเกิดปฏิกิริยาเคมี เฉลยข้อสอบหลังเรียน เรื่อง มวล พลังงานกับการเกิดปฏิกิริยาเคมี
- 23. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ตัวอย่างการบันทึกกิจกรรม 2.2 มวลกับการเกิดปฏิกิริยาเคมี สมาชิกในกลุ่ม 1. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 2. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 3. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 4. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 5. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 6. ชื่อ..................................................................................................ชั้น.................เลขที่..................... จุดประสงค์ของกิจกรรม เมื่อทากิจกรรมนี้แล้ว นักเรียนควรจะสามารถ 1. ทดลองและอธิบายได้ว่า ผลรวมมวลของสารตั้งต้นที่เข้าทาปฏิกิริยาเคมีเท่ากับผลรวมมวลของสาร ผลิตภัณฑ์ที่เกิดขึ้น 2. อธิบายได้ว่า ในระบบเปิดมวลของสารผลิตภัณฑ์มีการแลกเปลี่ยนกับสิ่งแวดล้อม วัสดุอุปกรณ์และสารเคมี รายการ ปริมาณ/กลุ่ม 1. บีกเกอร์ขนาด 250 cm3 2. หลอดทดลองขนาดกลาง 3. เครื่องชั่ง 4. หลอดทดลองขนาดใหญ่ พร้อมจุกยาง 5. สารละลายแบเรียมคลอไรด์ ความเข้มข้น 0.1 mol/dm3 6. สารละลายโซเดียมซัลเฟต ความเข้มข้น 0.1 mol/dm3 7. สารละลายกรดไฮโดรคลอริก ความเข้มข้น 0.1 mol/dm3 8. เม็ดหินปูนเล็กๆ 1 ใบ 2 หลอด 1 เครื่อง 1 หลอด 5 cm3 5 cm3 10 cm3 2 กรัม (5-8 เม็ด) 20
- 24. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี วิธีทดลอง ตอนที่ 1 1. ชั่งบีกเกอร์ และหลอดทดลอง 2 หลอด โดยหลอดทดลองที่ 1 บรรจุสารละลายแบเรียมคลอไรด์ หลอดทดลองหลอดที่ 2 บรรจุสารละลายโซเดียมซัลเฟต วางในบีกเกอร์และบันทึกมวลของบีกเกอร์ และหลอดทดลองทั้งสองที่บรรจุสารละลายแล้ว 2. เทสารละลายหลอดที่ 1 ลงในหลอดที่ 2 วางหลอดเปล่าไว้ที่เดิม สังเกตการเปลี่ยนแปลง 3. ชั่งบีกเกอร์ และหลอดทดลองทั้งสองอีกครั้ง เปรียบเทียบกับมวลที่ชั่งครั้งแรก การชั่งบีกเกอร์ และหลอดทดลอง 2 หลอด ที่บรรจุสารละลายแล้ว ตอนที่ 2 1. ชั่งบีกเกอร์ ที่ใส่เม็ดหินปูนประมาณ 5 – 8 เม็ด และหลอดทดลองขนาดใหญ่ที่บรรจุสารละลายกรด ไฮโดรคลอริกเจือจาง 10 cm3 พร้อมจุกยางปิดหลอดดังภาพ บันทึกมวล 2. นาเม็ดหินปูนใส่ลงในหลอดทดลองที่บรรจุกรด และปิดจุกยากทันที สังเกตการเปลี่ยนแปลง 3. ตั้งทิ้งไว้จนปฏิกิริยาสิ้นสุด ชั่งบีกเกอร์ และหลอดทดลอง พร้อมจุกยากอีกครั้ง บันทึกมวล 4. เปรียบเทียบมวลที่ชั่งในข้อ 3 กับมวลในข้อ 1 การชั่งบีกเกอร์ที่ใส่เม็ดหินปูน และหลอดทดลองขนาดใหญ่ที่บรรจุกรดแล้ว 21
- 25. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ตัวอย่างผลการทดลอง ตอนที่ มวลรวมของสารก่อนนามาผสม (กรัม) มวลรวมของสารหลังผสมกันแล้ว (กรัม) 1 142.5 142.5 2 164.5 164.5 คาถามท้ายการทดลอง 1. ในการทดลองตอนที่ 1 มวลของสารก่อนทาปฏิกิริยา และมวลของสารหลังทาปฏิกิริยาเท่ากันหรือไม่ แนวคาตอบ มวลของสารก่อนเกิดปฏิกิริยาและมวลของสารหลังเกิดปฏิกิริยาเท่ากันในการทดลอง 2. ถ้าไม่ปิดจุกหลอดทดลองขณะเกิดปฏิกิริยาระหว่างกรดกับหินปูน มวลของสารที่ชั่งได้ก่อนเกิด ปฏิกิริยาและหลังปฏิกิริยาแตกต่างกันหรือไม่ เพราะเหตุใด แนวคาตอบ แตกต่างกัน เพราะปฏิกิริยาระหว่างกรดกับหินปูนจะเกิดแก๊สคาร์บอนไดออกไซด์เป็น สารผลิตภัณฑ์ หากไม่ปิดจุกหลอดทดลองแก๊สคาร์บอนไดออกไซด์ที่เกิดขึ้นจะแพร่กระจายในอากาศ ทาให้มวลของสารที่ชั่งก่อนเกิดปฏิกิริยาไม่เท่ากับมวลของสารหลังเกิดปฏิกิริยา อภิปรายผลการทดลอง โซเดียมซัลเฟตเมื่อรวมกับแบเรียมคลอไรด์จะเกิดตะกอนสีขาวขุ่น และเมื่อชั่งมวลรวมของสารทั้ง 2 ที่บรรจุในภาชนะก่อนเกิดปฏิกิริยาเคมี และมวลรวมของผลิตภัณฑ์หลังเกิดปฏิกิริยาพร้อมกับภาชนะ พบว่า มีมวลเท่ากัน ส่วนปฏิกิริยาระหว่างเม็ดหินปูนกับกรดไฮโดรคลอริกเจือจาง มวลของหินปูนกับสารละลายกรด ไฮโดรคลอริกเจือจาง และหลอดทดลองที่บรรจุสารกับจุกยางรวมกันก่อนที่จะนามาใส่ในหลอดทดลองจะ เท่ากับมวลของผลิตภัณฑ์ที่เกิดขึ้นอยู่ภายในภาชนะและเม็ดหินปูนที่เหลืออยู่ สรุปผลการทดลอง มวลรวมของสารตั้งต้นที่นามาทาปฏิกิริยากันจะเท่ากับมวลรวมของผลิตภัณฑ์ที่เกิดขึ้น 22
- 26. เอกสารประกอบการจัดกิจกรรมการเรียนรู้แบบวัฏจักรการสืบเสาะหาความรู้ 7 ขั้น เรื่อง การเปลี่ยนแปลงพลังงานและการเกิดปฏิกิริยาเคมี ตัวอย่างการบันทึกกิจกรรม 2.3 พลังงานกับการเกิดปฏิกิริยาเคมี สมาชิกในกลุ่ม 1. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 2. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 3. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 4. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 5. ชื่อ..................................................................................................ชั้น.................เลขที่..................... 6. ชื่อ..................................................................................................ชั้น.................เลขที่..................... จุดประสงค์ของกิจกรรม เมื่อทากิจกรรมนี้แล้ว นักเรียนควรจะสามารถ 1. ทดลองและอธิบายได้ว่า ในการเกิดปฏิกิริยาเคมีจะมีพลังงานเข้ามาเกี่ยวข้อง 2. อธิบายเกี่ยวกับปฏิกิริยาดูดพลังงานและปฏิกิริยาคายพลังงานได้ วัสดุอุปกรณ์และสารเคมี รายการ ปริมาณ/กลุ่ม 1. ถ้วยกระเบื้อง 2. แท่งแก้วคนสาร 3. หลอดหยด 4. โพแทสเซียมเปอร์แมงกาเนต 5. น้าตาลทราย 6. แคลเซียมไฮดรอกไซด์ 7. แอมโมเนียมคลอไรด์ 8. น้ากลั่น 9. กระดาษลิตมัสสีแดงและสีน้าเงิน 10. ช้อนเบอร์ 1 2 ถ้วย 2 อัน 1 อัน 2 ช้อนเบอร์ 1 2 ช้อนเบอร์ 1 2 ช้อนเบอร์ 1 2 ช้อนเบอร์ 1 50 cm3 2 ชิ้น 4 อัน 23
